Bir etkinlik yapalım
Ekinlik için kullanacağımız malzemeler:
- Limon
- Sirke
- Karbonat
- Saf su
- Çamaşır suyu
- Bir kaç tane Karalahana yaprağı
Öncelikle hazırladığımız karalahana yaprağını bir süre sıcak suda bekletelim böylece karalahana suyunu elde edebileceğiz. Elde ettiğimiz karalahana suyunu beş ayrı şişeye boşaltıp A, B, C, D ve E şeklinde isim verelim

sonrasında aşağıdaki tabloyu çizelim
| Kullanılan malzemeler | Karalahana suyunda renk değişimi |
|---|---|
| Limon | |
| Sirke | |
| Karbonat | |
| Saf su | |
| Çamaşır suyu |
Ardından aşağıdaki çalışmaları yapalım
- A şişesine bir miktar limon sıkalım
- B şişesine sirke dökelim
- C şişesine biraz karbonat dökelim
- D şişesine saf su ekleyelim
- E şişesine ise çamaşır suyundan az miktarda ekleyelim ve gözlemlerimizi yukarıdaki tabloya kaydedelim
Etkinlik sonunda aşağıdaki duruma benzer bir sonuç elde ederiz.





Yukarıdaki gözlemlerimiz sonunda tablomuz ise şu şekilde olacaktır.
| Kullanılan malzemeler | Karalahana suyunda renk değişimi |
|---|---|
| Limon | Su kırmızı – pembe renk aldı |
| Sirke | Su kırmızı – pembe renk aldı |
| Karbonat | Su mavi – yeşil renk aldı |
| Saf su | Suda her hangi bir renk değişimi olmadı |
| Çamaşır suyu | Su başlangıçta yeşil oldu sonra sarı renk aldı |
Etkinlik sonucunda bazı maddelerin karalahana suyunda pembe – kırmızı renk verirken, bazılarının mavi – yeşil-sarı renk verdiğini gördük.
Bazı maddeler ise herhangi bir renk değişimine neden olmamıştır.
Asitler
Yaptığımız etkinlikte limon, sirke gibi maddelerin karalahana suyunda kırmızı - pembe renk verdiklerini gözlemledik. Bu maddeler asit özelliği gösteren maddelerdir. Eğer bu iki maddenin tadına baksaydık her ikisinin de ekşi tatlara sahip olduklarını görecektik.
O halde asitleri; tatlı ekşi olan ve karalahana suyunda kırmızı renk veren maddeler olarak tanımlayabildiğimiz gibi onları, sulu çözeltilerde ortama H+ iyonu veren maddeler olarak tanımlamak da mümkündür.
Örnek:
- H2SO4 -> 2H+ + SO42-
- HCl -> H+ + Cl-
- HNO3 -> H+ + NO3-
dikkat edilirse verilen tüm asitlerin sulu çözeltileri ortama H+ iyonu vermiştir.
a. Asitlerin genel özellikleri
- Asitlerin tatları ekşidir
- Bazlar ile tepkimeye girerek tuz ve su oluştururlar
- Karalahana suyunda pembe – kırmızı renk verirler
- Mavi turnusol kağıdını kırmızıya boyarlar
- Sulu çözeltileri elektrik akımını iletir
- Yakıcı ve tahriş edicidirler
- Metaller ile tepkimeye girerek H2 gazı çıkışına neden olurlar
- 1
b. Asit özelliği gösteren bazı maddeler
| Kimyasal Adı | Formülü | Yaygın Adı |
|---|---|---|
| Sülfürik Asit | H2SO4 | Zaç yağı |
| Hidroklorik Asit | HCl | Tuz ruhu |
| Nitrik Asit | HNO3 | Kezzap |
| Sitrik Asit | C6H8O7 | Limon Asidi |
| Asetik Asit | CH3COOH | Sirke Asidi |
| Malik Asit | C4H6O5 | Elma Asidi |
| Formik Asit | CH2O2 | Karınca Asidi |
Bazlar
Sulu çözeltilerinde ortama OH– (Hidroksit) iyonu veren maddelerdir.
Yaptığımız etkinlikte Karalahana suyunda mavi-yeşil renk veren maddeler bazik özellik gösteren maddelerdir.

- KOH -> K+ + OH–
- Ca(OH)2 -> Ca2+ + 2OH–
a. Bazların genel özellikleri
- Karalahana suyunda mavi-yeşil-sarı renk verirler
- Kırmızı turnusol kağıdını maviye boyarlar
- Genellikle temizlik malzemesi olarak kullanılırlar
- Sulu çözeltilerinde suya OH– iyonu verirler
- Asitlerle tepkimeye girerek tuz ve su oluşumuna neden olurlar
- Metal ve cam eşyalarda matlaşmaya neden olurlar
- Sulu çözeltileri elektrik akımını iletir
- 1
b. Baz özelliği gösteren bazı maddeler
| Kimyasal Adı | Formülü | Yaygın Adı |
|---|---|---|
| Sodyum Hidroksit | NaOH | Sud kostik |
| Potasyum Hidroksit | KOH | Potas kostik |
| Amonyak | NH3 | Amonyak |
| Kalsiyum Hidroksit | Ca(OH)2 | Sönmüş kireç |
pH Metre
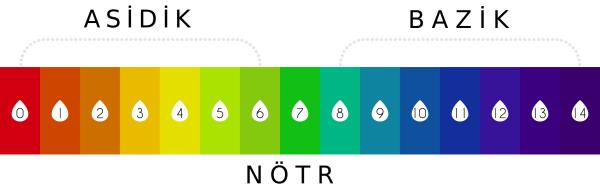
Maddelerin asidik ya da bazik değerlerini gösteren ve 0 – 14 arasında değer alan bir cetveldir.
pH cetvelinin özellikleri şunlardır;
- 0-7 arası maddenin asidik olduğunu gösterir. Sıfıra yaklaştıkça asidik özellik artar
- 7-14 maddenin bazik olduğunu gösterir. 14’e yaklaştıkça bazik özellik artar
- 7 maddenin nötr olduğunu gösterir. Asidik ya da bazik özellik göstermeyen maddelerin pH değeri 7’dir.
Asit Yağmurları
Havaya karışan bazı gazların atmosferdeki su ile tepkime oluşturarak asit şeklinde yer yüzüne inmesi sonucunda asit yağmurları meydana gelir.
Asit yağmurları, hava karışan kirleticiye ve karışma miktarına göre değişebilmektedir.
Aşağıda havaya karışan kirleticiler ve tepkime sonucunda oluşturdukları asit türü verilmiştir.
| Kirletici | Oluşturduğu Asit Türü |
|---|---|
| NO2 (Azotdioksit) | HNO3 (Nitrik Asit – Kezzap) |
| SO2 (Kükürtdioksit) | H2SO4 (Sülfürik Asit – Zaç yağı) |


